Insuficienţa hipofizară
©
Autor: Andrei Mihai-Gabriel
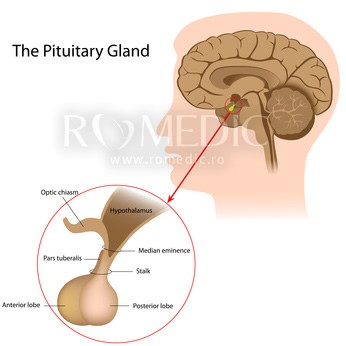
Anatomia şi fiziologia hipofizei
Hipofiza sau glanda pituitară este o parte esenţială a sistemului endocrin denumită și master gland, întrucât controlează secreţia majorităţii glandelor sistemului endocrin.Are dimensiuni reduse (diametru între 1-1.5 cm, greutate 0.5-1 g) și este localizată la baza encefalului, la nivelul şeii turceşti a osului sfenoid.
Hipofiza este alcătuită din adenohipofiză sau lobul anterior (2/3 din hipofiză) şi neurohipofiză sau lobul posterior, având origine embriologică diferită. Lobul intermediar (situat între cele două) este slab dezvoltat la om (aproximativ 1% din hipofiză). Adenohipofiza este partea care deţine funcţie secretorie, în timp ce neurohipofiza are doar rol de depozit şi eliberare în circulaţie a hormonilor produşi la nivel hipotalamic.
Secreţia hormonală a adenohipofizei este reglată de hipotalamus (prin hormoni stimulatori şi inhibitori) şi de hormonii secretaţi prin stimularea gladelor din periferie. Controlul hipotalamic se face prin hormoni stimulatori (liberine) şi inhibitori (statine). Hormonii periferici exercită un feedback pozitiv (stimularea de către estradiolul produs la nivelul ovarului a secreţiei de hormon luteinizant, mecanism ce stă la baza ovulaţiei) sau feedback negativ (inhibarea secreţiei de hormoni hipofizari de nivelele crescute de hormoni corespondenţi ai glandelor periferice)
Din punct de vedere anatomic şi funcţional, relaţia intre hipotalamus şi hipofiză se poate sistematiza in două unităţi distincte şi anume: sistemul hipotalamo-neurohipofizar şi sistemul hipotalamo-adenohipofizar.
Sistemul hipotalamo-neurohipofizar
Nucleii magnocelulari din hipotalamus sunt cei care produc ADH (hormonul antidiuretic ce împiedică pierderea excesivă de apă prin urină) şi oxitocina (stimulează contracţia uterului şi expulzia laptelui din glanda mamară). Axonii acestora trec prin tija pituitară ajungând la nivelul neurohipofizei. Hormonii produşi la nivel hipotalamic sunt transportaţi prin axoni la neurohipofiză unde sunt depozitaţi. Prin urmare se înţelege că neurohipofiza nu are funcţie secretorie, având doar rol de depozit pentru hormonii hipotalamici pe care îi eliberează în circulaţie în fucnţie de necesităţile organismului.Sistemul hipotalamo-adenohipofizar
Nucleii parvocelulari hipotalamici secretă aşa-numiţii hormoni hipofizotropi care stimulează sau inhibă secreţia hipofizară.Hormonii stimulatori, numiţi şi liberine, sunt reprezentaţi de:
- somatoliberina (GHRH-growth hormone releasing hormone) -stimulează secreţia de GH (growth hormone-hormonul de creştere sau STH-hormon somatotrop) ;
- tiroliberina (TRH) - stimulează secreţia de TSH (thyroid stimulating hormone) şi prolactină (PRL) ;
- corticoliberina (CRH) -reglează secreţia de ACTH (adrenocorticotropic hormone) ;
- gonadoliberina (GnRH) -control secreţie FSH (hormonul foliculo-stimulant) şi LH (hormonul luteinizant) .
Hormonii hipotalamici inhibitori sunt somatostatina (SS), ce inhibă secreţia GH şi dopamina-inhibă secreţia prolactinei.
Hormonii reglatori hipotalamici ajung la nivelul adenohipofizei transportaţi prin sistemul port hipotalamo-hipofizar. Acest sistem este format din capilare şi vase portale lungi. Capilarele au peretele fenestrat - pot intra şi ieşi hormonii. Astfel, la nivel hipotalamic, hormonii pătrund în capilarele de la acest nivel, ce se unesc formând vasele portale lungi (fără perete fenestrat) - localizate la nivelul tijei pituitare. Ajunse la adenohipofiză, vasele se capilarizează, din nou au fenestre ce permit ieşirea hormonilor şi acţiunea asupra celulelor adenohipofizei.
Hormonii adenohipofizari
Hormonii adenohipofizari sunt eliberaţi în sânge, ajung la nivelul receptorilor membranari ai celulelor ţintă, asupra cărora determină efecte specifice. Din punctul de vedere al acţiunii, produşii de secreţie hipofizară pot fi împărţiţi în hormoni cu acţiune directă (GH şi PRL) şi cei cu acţiune indirectă - prin stimularea secreţiei hormonale a altor glande (TSH, CRH, FSH şi LH).
- GH (sau hormonal somatotrop STH) acţionează fie direct, fie indirect (prin factorul de creştere insulin-like IGF-1 a cărui sinteză hepatică o stimulează) determinând creşterea în înălţime a corpului şi influenţând metabolismul organismului; secreţia sa maximă se realizează în timpul somnului;
- prolactina (PRL) - fiziologic este secretată doar în sarcină (pregăteşte glanda mamară pentru lactaţie) şi alăptare (stimulează producţia de lapte matern);
- hormonul stimulator al tiroidei (TSH) are rolul de a creşte secreţia hormonilor tiroidieni, de a stimula creşterea vascularizaţiei şi a volumului tiroidei;
- hormonul adrenocorticotrop (ACTH) se secretă sub formă de proopiomelanocortină (POMC), alături de hormonul melanocito-stimulator (MSH-rol în pigmentarea cutanată); ACTH are rolul de a stimula secreţia glandei suprarenale, anume a hormonilor glucocorticoizi si androgeni (în mai mică măsură-stimulează secreţia de mineralocorticoizi); stimulează şi troficitatea glandei;
- hormonii gonadotropi (foliculo-stimulant FSH şi luteinizant LH) au acţine diferită în funcţie de sex; FSH la femeie stimulează secreţia estrogenului şi maturarea foliculului ovarian, iar la bărbaţi stimulează formarea spermei; LH la femei declanşează ovulaţia şi stimulează secreţia de hormoni androgeni, iar la bărbați stimulează sinteza de testosteron.
Cauze și factori de risc
Cauzele insuficienţiei hipofizare sunt multiple. Cel mai frecvent incriminat este adenomul hipofizar (tumoră benignă) şi tratamentul acestuia - chirurgia adenohipofizei (în special abordul transparietal) sau radioterapia acesteia.Clasificarea etiologiilor posibile poate fi făcută după criterii anatomice (localizarea hipotalamică sau hipofizară), clinice (acută sau cronică), precum şi în funcţie de vârsta la care se instalează deficitul (copil sau adult).
Criteriul anatomo-topografic
1. Cauze hipotalamice - orice factor nociv care interferă cu producţia de liberine hipotalamice sau care scad producerea hormonului antidiuretic şi a ocitocinei.2. Afecţiuni ale tijei pituitare (asigură comunicarea hipotalamo-hipofizară) care interferă cu transportul hormonilor hipotalamici la hipofiză. Particularitatea în acest caz este apariţia hiperprolactinemiei de defrenare-prolactina creşte pe baza absenţei dopaminei (hormon hipotalamic inhibitor al secreţiei de prolactină) .
3. Cauze hipofizare (primare)
- Formaţiuni tumorale - adenomul hipofizar (tumoră benignă dezvoltată din celulele hipofizei) este cea mai frecventă cauză a insuficienţei hipofizare. Mecanismul patogenetic este injuria celulelor hipofizare prin comprimarea vaselor sistemului port hipotalamo-hipofizar sau comprimarea directă a celulelor hipofizare. Macroadenoamele (dimensiuni peste 1 cm) sunt capabile de acest efect. Microadenoamele (sub 1 cm) determină foarte rar insuficienţă hipofizară. Adenomul poate fi clinic funcţional - secretă în exces unul sau mai mulţi hormoni hipofizari, manifestându-se clinic prin efecte ale excesului hormonal şi ale insuficienţei celorlalţi hormoni. Când este clinic nefuncţional (nu secretă hormoni activi) tabloul clinic prezintă doar semnele insuficienţei hipofizare. Orice alte formaţiuni intracraniene pot determina sindrom de insuficienţă hipofizară prin efect de masă asupra hipotalamusului sau hipofizei (exemplu craniofaringiomul, dezvoltat dintr-un rest embrionar al pungii lui Rathke).
- Cauze iatrogene - în urma intervenţiilor medicale - chirurgia sau radioterapia unei formaţiuni tumorale hipofizare pot fi urmate de instalarea insuficienţei, incidenţa variind în funcţie de dimensiunea tumorii, caracterul infiltrativ al acesteia, abordul chirurgical sau tipul de radioterapie. Intervenţia pentru alte formaţiuni intracraniene se poate solda cu insuficienţă hipofizară. (7)
- Mutaţii genetice - hipopituitarism congenital. O serie de gene implicate în dezvoltarea hipofizei pot avea mutații, cu apariţia aplaziei pituitare (lipseşte hipofiza), hipoplaziei pituitare (dimunsiuni şi funcţie scăzută a glandei hipofize), ectopie hipofizară.
- Traumatisme (ex. accidente sau sporturi de contact) care pot rupe tija pituitară sau pot afecta hipofiza.
- Afecţiuni vasculare (ischemia şi hemoragia). Ischemia hipofizară cu necroză consecutivă la femeia postpartum este cunoscută sub denumirea de sindrom Sheehan. În perioada gravidităţii, hipofiza se hipertrofiază (creşte), astfel că o hemoragie masivă la naştere ce determină hipovolemie marcată, va determina o ischemie a glandei hipofize. Cele mai afectate celule sunt cele lactotrope, în consecinţă, suspiciunea instalării acestui sindrom apare în situaţia în care femeia nu prezintă secreţie lactată după naştere (prin absenţa prolactinei). (6) Hemoragia (apoplexia) hipofizară apare mai frecvent la nivelul unui adenom hipofizar. Poate apărea şi în cazul unei coagulopatii congenitale sau dobândite (ex. tratament incorect cu anticoagulante).
- Infecţii precum sifilisul, tuberculoza sau alte tipuri de infecţii ce pot afecta hipofiza.
- Hipofizita autoimună reprezintă infiltrarea hipofizei cu limfocite şi plasmocite producătoare de auto-anticorpi. Tratamentul cu anticorpi monoclonali (ex. Ipilimumab în mielomul multiplu) se asociază cu o frecvenţă mai ridicată a acestei patologii. (1)
- Infiltraţiile hipofizei în cadrul unor boli ca hemocromatoza, hemopatiile maligne (leucemii, limfoame), histiocitoză, sarcoidoză.
- Sindromul de şa turcică goală. (3) Hipofiza apare comprimată la efectuarea unui IRM (imagistică prin rezonanţă magnetică) de către arahnoida (parte a meningelui) herniată la acest nivel. Pe radiografie, datorită lichidului cefalorahidian care umple hernierea arahnoidei, locul hipofizei apare gol, de unde şi denumirea sindromului.
Criteriul clinic
1. AcuteDebut brusc, rapid al insuficienţei, cu mortalitate crescută, în special prin deficitul de hormon corticotrop (ACTH) şi insuficienţa corticosuprerenaliană consecutive. Tratamentul se face cu hidrocortizon administrat de urgenţă.
Cauzele mai frecvente sunt sindromul Sheehan, apoplexia pituitară, inflamaţii acute ale hipofizei.
2. Cronice
Reprezintă tipul cel mai frecvent de instalare a insuficienţei hipofizare. Diagnosticul clinic se pune tardiv, modificările instalându-se lent progresiv.
Vârsta la care apare deficitul hormonilor hipofizari
Vârsta la care apare deficitul hormonilor hipofizari determină felul în care acesta se manifestă pe plan clinic, în special prin deficitul de hormon de creştere şi hormoni gonadotropi.- Deficitul de hormon de creştere la copil determină apariţia nanismului hipofizar. Se caracterizează prin oprirea creşterii cu hipostatură semnificativă (statura finală 1.20-1.30 m)
- La adult, insuficienţa hipofizară se manifestă clinic variat în funcţie de linia hormonală deficitară.
Fiziopatologie
Scăderea nivelului hormonilor hipofizari în organism determină un deficit de hormoni ai glandelor pe care le controlează. Deşi în mod normal acest deficit al hormonilor periferici ar stimula, prin feedback negativ, secreţia hipofizară, în cazul insuficienţei hipofizare glanda nu este capabilă de un răspuns adecvat.Manifestări clinice
Tabloul clinic este diferit în funcţie de hormonii deficitari, de modul în care se instalează deficitul (acut sau cronic), precum şi în funcţie de patologia care determină insuficienţa. Deficitul hipofizar poate fi unihormonal (ex. deficit de hormon de creştere) sau poate implica toţi hormonii hipofizari, când poartă denumirea de panhipopituitarism. Datorită dispoziţiei celulelor hipofizare, insuficienţa se instalează de obicei respectând o anumită ordine: liniile lactotropă şi somatotropă sunt afectate primele, urmate de insuficienţa gonadotropă, insuficienţa tirotropă, ultima fiind cea cortiotropă. (8)Insuficienţa hipofizară acută este o urgenţă prin deficitul de ACTH care determină criza adrenală - insuficienţă corticosuprarenală de tip central (secundară). (4) Pacientul prezintă: durere de cap brusc instalată, ce poate orienta medicul spre o patologie hipofizară, greţuri, vărsături, hipotensiune şi hiponatrienie. Poate apărea, de asemeneaa deficitul acut de hormon antidiuretic, manifestat prin poliurie şi polidipsie. În rest, ceilalţi hormoni hipofizari vor determina modificări clinice mai târziu în cursul evoluţiei sindromului.
În majoritatea cazurilor, debutul este cronic, insidios, manifestările clinice variind în funcţie de vârsta pacientului.
1. Deficitul de hormon de creştere (GH)
- La copil, deficitul de hormon de creştere, asociat sau nu cu deficitul altor hormoni, determină nanismul hipofizar. Creşterea se realizează cu întârziere, iar talia copilului este scăzută în raport cu talia corespunzătoare vârstei şi sexului. Talia maximă pe care o poate atinge nu depăşeşte 1, 30 m. Corpul este normal proporţionat. Apar faciesul de copil, acromicirie (extremităţile sunt mici) şi microsplanhnie (organe interne de dimensiuni mici). Sistemul muscolo-scheletal este slab dezvoltat, cu risc crescut de osteoporoză. Psihic şi intelectual, dezvoltarea este normală (când nu este prezentă insuficienţa tireotropă care poate determina tulburări neurologice).
- La adult, deficitul de hormon de creştere determină tulburări nespecifice, care trec adesea neobservate. Astfel, apar oboseala, reducerea capacităţii de efort, tulburări psihice care pot merge până la depresie. (5) Creşte riscul cardiovascular prin creşterea colesterolului şi riscul de fractură prin scăderea efectului anabolic al hormonului de creştere (GH promovează sănătatea oaselor).
2. Deficitul de FSH şi LH
La ambele sexe determină reducerea libidoului, scăderea fertilităţii şi pierderea dispoziţiei caracteristice a pilozităţii. La sexul feminin apar tulburări ale ciclului menstrual, oligomenoree, amenoree, dispareunie (durere în timpul actului sexual); la bărbat, disfuncţie erectilă şi scăderea dimensiunii şi a funcţiei testiculare (atrofie testiculară).
3. Deficitul de ACTH
Insuficienţa suprarenală de cauză centrală (prin lipsa corticotropinei) se manifestă clinic asemănător bolii Addison, cu excepţia hiperpotasemiei (boala Addison asociază un deficit de aldosteron ce cauzează hiperpotasemia) şi a hiperpigmentării (în boala Addison nivelul de ACTH este ridicat prin absenţa feedback-ului negativ realizat de hormonii glucocorticoizi; întrucât molecula de ACTH se sintetizează dintr-un precursor comun (pro-opiomelanocortina) cu hormonul melanocito-stimulator (MSH) responsabil de pigmentarea cutanată, în boala Addison apare o hiperpigmentare a mocoaselor si a tegumentelor ce lipseşte în insuficienţa hipofizară). Clinic, bolnavul prezintă anorexie, greţuri, vărsături, diaree, dureri abdominale, articulare şi musculare, alterarea stării generale, oboseală, slăbiciune; hipoglicemia simptomatică şi alterarea funcţiei sexuale apar cu o frecvenţă mai redusă.
4. Deficitul de tireotropina (TSH) determină insuficienţa tiroidiană de tip central. Modificările clinice sunt cele ale hipotiroidismului cu: creştere în greutate nejustificată, piele uscată, căderea părului. Starea generală este alterată cu oboseală, sensibilitate crescută pentru temperaturile scăzute, constipaţie, rigiditate musculară, scăderea performanţelor intelectuale.
5. Deficitul de prolactină devine manifest în perioada postpartum (după naştere) când determină scăderea lactaţiei. Sindromul Sheehan (descris anterior) are ca manifestare principală absenţa lactaţiei datorită unui deficit de prolactină.
6. Insuficienţa hormonului antidiuretic (ADH) poate fi de asemenea întâlnită, pacientul prezentând poliurie şi polidipsie severe. Deficitul de ACTH poate masca diabetul insipid instalat prin faptul că lipsa lui determină o scădere a filtrării glomerulare, prin urmare scăzând diureza. Astfel, terapia pe linia hormonului ADH se va face după corecţia deficitului de glucocorticoizi.
Diagnostic
Abordarea clinică a pacientului cu insuficienţă hipofizară impune o serie de investigaţii menite să stabilească diagnosticul pozitiv, etiologia şi posibilele boli asociate.Diagnosticul pozitiv se pune prin explorarea funcţiei bazale a hipofizei (dozări hormonale) precum şi prin teste dinamice, de stimulare a secreţiei hipofizare. Dozarea hormonilor hipofizari nu reflectă exact funcţia hipofizară, valoarea acestora poate fi la limita inferioară a normalului, tabloul clinic sugerând însă deficitul, situaţie în care se impune utilizarea testelor dinamice. Acestea certifică diagnosticul, arătând absenţa rezervelor hormonale. Pentru GH se utilizază testul la hipoglicemie indusă prin insulină (hipoglicemia stimulează secreţia de hormon de creştere) sau testul la GHRH (hormonul hipotalamic de stimulare a secreţiei de GH); rezerva gonadotropă este evaluată prin testul la GnRH (hormonul eliberator al gonadotropinelor hipofizare); secreţia de ACTH este evaluată prin testul la CRH (hormonul hipotalamic al eliberării de ACTH); hipotiroidismul central din insuficienţa hipofizară este diagnosticat prin testul la TRH (hormonul hipotalamic al eliberării de TSH).
Diagnosticul etiologic
Cauzele insuficienţei hipofizare fiind multiple, prima intenţie este evaluarea imagistică a glandei pentru a exclude cauza cea mai frecventă, adenomul hipofizar. Astfel se recomandă efectuarea IRM hipofizar cu sau fără contrast sau a unei radiografii de şa turcească. În situaţia în care clinic apar semnele hipersecreţiei unui hormon hipofizar cu deficitul celorlalţi se suspectează un adenom hipofizar clinic funcţional. Când tabloul clinic înclină spre o boală ce evoluează cu infiltraţia hipofizei se evaluează biologic în acest sens (ex. determinarea feritinei şi a transferinei în hemocromatoză).Tratament
Se realizează subtituţia hormonilor deficitari sau a hormonilor glandelor periferice pe care le controlează. Aceasta se face în ordine inversă instalării deficitului, începându-se cu cortizolul. Cu excepţia GH şi a hormonilor necesari pentru fertilitate (GnRH, FSH, HCG) care se substituie direct, ceilalţi hormoni hipofizari nu se administrează direct, se substituie cu hormoni ai glandelor ţintă. Durata tratamentului de substituţie variază, toată viaţa pentru ACTH şi TSH, respectiv secvenţial pentru hormonii gonadotropi (pentru inducerea de menstre farmacologice). Hormonul de creştere se va administra înaintea celor gonadotropi care determină închiderea cartilajelor de creştere.Tratamentul etiologic se face prin neurochirurgie sau radioterapie pentru adenomul hipofizar; pentru celelalte cauze mai puţin frecvente tratamentul variază.
Din Biblioteca medicală vă mai recomandăm:
Forumul ROmedic - întrebări și răspunsuri medicale:
Pe forum găsiți peste 500.000 de întrebări și răspunsuri despre boli sau alte subiecte medicale. Aveți o întrebare? Primiți răspunsuri gratuite de la medici.- Probleme la nivelul hipofizei?
- Varsta osoasa mai mica decat varsta cronologica
- Macro adenom hipofizar - caut un raspuns urgent va rog!
- Hipofiza - ce analize ar fi necesare pentru a vedea daca hipofiza este sanatoasa?
- Hipofiza
- Glanda hipofiza