Anovulația cronică
Aspecte generale
Ovarele sunt două organe pereche care fac parte din organele genitale interne ale aparatului reproducător feminin. Funcţiile lor principale sunt: producerea de ovocite (ovogeneză) şi eliberarea gameţilor feminini (ovulaţie) şi secreţia hormonală (estrogeni, progesteron şi cantităţi scăzute de testosteron).
În fiecare lună, aproximativ în ziua a 14-a a ciclului menstrual are loc procesul de ovulaţie prin care ovocitul secundar este eliberat din foliculul matur şi este capabil de a fi fecundat, în mod normal, de un singur spermatozoid.
Ovulaţia nu are numai o componentă ovariană, ci şi una neuroendocrină, reprezentată de hipotalamus şi hipofiză. Astfel, în cadrul procesului de ovulaţie se poate vorbi despre o axă hipotalamo-hipofizo-ovariană. Comunicarea între elementele acestui circuit este realizată de hormoni. Cei mai importanţi hormoni ai circuitului sunt: hormonul eliberator de gonadotropine (Gn-RH), hormonul foliculostimulant (FSH), hormonul luteinizant (LH), estrogenul, progesteronul, inhibina şi testosteronul. Cu toate că mecanismele de interacţiune hormonală nu sunt elucidate în totalitate, totuşi, funcţionarea generală a acestei axe este bine înţeleasă. [1]
În cazul în care unul dintre elementele constitutive ale axei hipotalamo-hipofizo-ovariene este afectat de un proces patologic, apare anovulaţia, definită prin incapacitatea ovarelor de a asigura evoluţia foliculilor primordiali şi de a elibera ovocitul secundar. Atunci când factorul de agresiune, care determină anovulaţia acută, nu este sau nu poate fi înlăturat, se instalează anovulaţia cronică. Au fost identificate 4 subcategorii ale anovulaţiei cronice:
1. anovulaţia hiperprolactinemică (hipersecreţie de prolactină);
2. anovulaţia hipogonadotropă (secreţie insuficientă de FSH şi LH);
3. anovulaţia normogonadotropă (sinteză corespunzătoare de FSH şi LH, dar insuficientă de Gn-RH);
4. anovulaţia hipergonadotropă (sinteză şi secreţie crescută de FSH şi LH). [2]
Epidemiologie
Se consideră că fiecare femeie va avea, la un moment dat, în decursul perioadei fertile, un episod de anovulaţie. În privinţa anovulaţiei cronice, datele sunt cu atât mai greu de adunat, din cauza faptului că multe dintre persoanele afectate nu solicită ajutorul medicului. Spre exemplu, în SUA, se estimează un interval de 6-15% în rândul populaţiei de sex feminin, cu o vârstă ce permite purtarea unei sarcini. [3]
Anovulaţia cronică se corelează cu patologii precum: hiperinsulinemia (nivel sangvin de insulină ridicat), rezistenţa la insulină (deficit al receptorilor pentru insulină), faza incipientă a diabetului zaharat tip II (non-insulino dependent), dislipidemia (o cantitate anormală de lipide în sânge), boli cardiovasculare, hipertensiune, boli asociate aparatului genital feminin (hiperplazie sau cancer endometrial), boli neurologice (epilepsie). Se poate asocia şi cu medicaţia neuropsihiatrică (acid valproic). [4]
Simptomatologie
Anovulaţia cronică se manifestă prin următoarele semne specifice:
- absenţa sau tulburarea menstruaţiilor;
- hipersensibilitate la nivelul sânilor;
- creşterea dimensiunii abdomenului inferior;
- modificări comportamentale (depresie, anorexie, anxietate, bulimie, stres cronic). [5]
Această simptomatologie se dovedeşte a fi destul de vagă şi de cele mai mult ori medicul va efectua explorări suplimentare pentru a identifica substratul care a cauzat patologia. Astfel, în cursul examenului clinic, în funcţie de segmentul analizat, medicul ar putea identifica:
- modificări ale vocii (exemplu: în cazul hipersecreţiei de hormoni androgeni, vocea se poate îngroşa);
- acnee (determinată tot de un dezechilibru hormonal, când raportul dintre hormonii estrogeni şi hormonii androgeni este subunitar);
- acanthosis nigricans (pete întunecate ce apar: pe suprafaţa gâtului, la nivelul axilelor şi în porţiunea internă a coapselor);
- strii violacee apărute în porţiunea laterală a abdomenului (pe flancurile abdominale), semn caracteristic bolii Cushing;
- aspectul feţei poate fi „de lună plină” (sindrom Cushing)
- distribuţia părului (în cazul hiperandrogenismului se observă o hiperpilozitate la nivelul întregului corp, mai puţin la nivelul scalpului unde există riscul de dezvoltare a alopeciei; în cazul insuficienţei suprarenaliene, din cauza hipoandregenismului, pacienta pierde părul pubian şi axilar);
- ochii pot fi exoftalmici (hipertiroidie); se pot identifica tulburări sau pierderi ale câmpului vizual lateral (hemianopsie bitemporală), manifestări ale tumorilor hipofizare (adenoame sau prolactinoame);
- urechi disproporţionate sau cu dimensiuni mărite (acromegalie: hipersecreţie a hormonului de creştere – STH – după încheierea pubertărţii, ce conduce atât la tulburări destul de severe ale organelor interne, cât şi la dezvoltarea anormală a extremităţilor);
- gât scurt, exces de piele pe ceafă, pliu cutanat pe feţele laterale ale gâtului (semne specifice sindromului Turner);
hipertrofia tiroidei; - modificări ale conformaţiei sânilor şi galactoree (hiperprolactinemie);
- raportul de distribuţie a grăsimii (talie/şolduri) modificat (obezitate, sindrom Cushing, etc. )
- modificări ale mucoasei vaginale (ex: uscarea mucoasei vaginale) datorate hipoestrogenizării. [6], [7], [8]
Cauze
Anovulaţia hiperprolactinemică
Prolactina este un hormon secretat de hipofiza anterioară (adenohipofiza). Hiperprolactinemia este reprezentată de creşterea concentraţiei serice a acestui hormon până la valori de 400-500 UI (unităţi internaţionale) /l sau 20-25 ng/ml. Hiperprolactinemia este produsă de:
- prolactinoame (tumori hipofizare producătoare de prolactină);
- tumori hipofizare care blochează funcţionarea normală a hipotalamusului;
- boli endocrine: hipotiroidism primar (hormonul eliberator al tireotropinei sau TRH determină secreţia de prolactină); sindromul ovarelor polichistice (scade nivelul FSH-ului ce duce la tulburări ale procesului de foliculogeneză);
- medicamente: neuroepileptice (fenotiazine), antidepresive (dibenzazepine), antihipertensive (reserpină), estrogen în doze crescute.
Hiperprolactinemia afectează:
- maturarea foliculară şi steroidogeneza;
- ovulaţia;
- procesul de luteinizare (formarea corpului galben);
- funcţionarea normală a corpului galben/luteal.
Hiperprolactinemia este corelată cu episoade de ovulaţie spontană ce pot determina apariţia sarcinilor.
Anovulaţia hipogonadotropă
Se caracterizează printr-o sinteză defectuoasă de gonadotropine (FSH şi LH). Poate fi asociată cu diminuarea simţului olfactiv şi atunci diagnosticul va fi de sindrom Kallmann.
Cauza cea mai frecventă este stresul emoţional acut sau cronic. Mecanismul fiziopatologic prin care stresul determină inhibiţia ovulaţiei este următorul: în prezenţa unui agent stresor, hipotalamusul va sintetiza şi elibera în circulaţie hormonul eliberator de corticotropină (CRH). Acesta va stimula la nivelul hipofizei secreţia şi sinteza hormonului adrenocorticotrop (ACTH) care va acţiona asupra corticalei suprarenaliene şi va induce secreţia de cortizol. Cortizolul circulant va reduce efectele: hormonului luteinizant (LH), estradiolului (estrogen) şi progesteronului şi va inhiba producţia de hormon eliberator al gonadotropinelor (Gn-RH), astfel producându-se tulburări ale ovulaţiei.
Poate fi asociată şi cu: adenoame hipofizare, craniofaringioame, ischemie şi necroză hipofizară.
Anovulaţia normogonadotropă
Pacientele nu sunt hipoestrogenice (produc cantităţi normale de hormoni estrogeni), însă problema vizează secreţia intermitentă, firească, de Gn-RH. Este asociată, în general, cu sindromul ovarelor polichistice.
Cauza principală a sindromului ovarelor polichistice este perturbarea dezvoltării histologice şi funcţionale a foliculilor secundari (antrali). La stadiul de maturare ajung mai mulţi foliculi secundari, în locul unuia singur, iar existenţa acestor foliculi multipli conduce la creşterea concentraţiei sangvine de estradiol (estrogen) care va inhiba eliberarea de hormon foliculostimulant (FSH) şi astfel este inhibată foliculogeneza. Ca urmare a examinării complete a pacientei (clinică şi de laborator), pot fi indicate următoarele simptome: nivel seric crescut de hormoni androgeni (determină anovulaţie), intoleranţă la glucoză, globulină de legare a hormonilor sexuali scăzută (SHBG), alterări ale menstruaţiei, acnee, hirsutism, subfertilitate, uşoară creştere în greutate, disfuncţii tiroidiene şi suprarenaliene.
Anovulaţia hipergonadotropă
Sunt înregistrate niveluri crescute de FSH (hormon foliculostimulant) şi LH (hormon luteinizant). Este determinată hipertrofia celulelor hipofizare sau de injuria vasculară a adenohipofizei. Cauzele sunt reprezentate de: tumori hipofizare (micro sau macroadenoame), sarcoidoză şi ischemie (apoplexie pituitară). Suprastimularea ovariană consecutivă va determina infertilitate. [2], [6], [9]
Mecanism fiziopatologic general
Iniţierea ciclului ovarian este dependentă de sinteza şi secreţia hormonului stimulator al gonadotropinelor (Gn-RH) de către neuronii nucleului arcuat hipotalamic. Mai departe, acest hormon va fi eliberat, în mod pulsatil, în vasele sistemului port hipotalamo-hipofizar, localizate la nivelul tijei pituitare, şi va ajunge în hipofiza anterioară (adenohipofiză), unde va determina producţia, în celulele adenohipofizei, de hormon foliculostimulant (FSH) şi hormon luteinizant (LH).
Hormonul foliculostimulant produce foliculogeneza. Prin acest proces se înţelege că un număr de foliculi primordiali (alcătuiţi dintr-un ovocit primar şi celule foliculare ce înconjoară ovocitul primar) vor începe să se diferenţieze, urmărind trei stadii evolutive: stadiul de folicul primar (unilamelar şi apoi multilamelar), stadiul de folicul secundar/antral şi, în final, stadiul de folicul matur/de Graaf. În fiecare lună, numai un singur folicul primordial va putea să se matureze (să atingă stadiul de folicul matur), ceilalţi foliculi suferind un proces de atrezie (involuţie). Totodată, foliculul primordial care a intrat în procesul de evoluţie va elibera inhibina, hormon care inhibă secreţia de FSH.
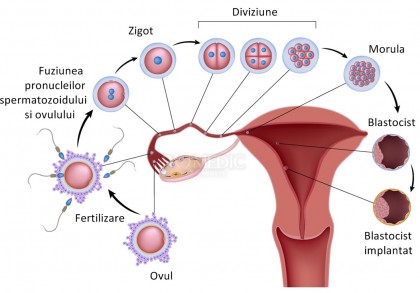
În urma dezvoltării foliculare, ovocitul primar va suferi o serie de modificări genetice, în urma cărora va deveni ovocit secundar, ce va dobândi un bagaj cromozomial corespunzător menit ca, în urma fecundării de către spermatozoid, să conducă la evoluţia normală a embrionului şi, mai apoi, a fătului. De asemenea, celulele foliculare înconjurătoare vor secreta cantităţi importante de estrogeni care vor produce un efect de feedback pozitiv asupra hipofizei, în urma acestui proces secretându-se cantităţi importante de LH (hormon luteinizant) care vor produce un vârf al LH-ului. La 24-48 de ore după acest vârf (în jurul zilei a 14-a a ciclului menstrual) se va produce ovulaţia, caracterizată prin ruptura foliculului matur şi expulzia ovocitului secundar.
După încheierea procesului de ovulaţie, ceea ce rămâne din foliculul matur se va transforma în corp luteal. Celulele luteale vor continua să secrete estrogeni, progesteron şi inhibine, menţinându-se în acest mod un nivel scăzut de Gn-RH, FSH şi LH. Dacă ovocitul secundar nu a fost fecundat, corpul luteal va degenera, se va fibroza şi se va transforma în corp alb.
În jurul zilei a 28-a a ciclului menstrual normal se produce menstruaţia. Întrucât nu mai există nicio influenţă hormonală inhibitorie asupra hipotalamusului şi a hipofizei, axa hipotalamo-hipofizo-ovariană îşi recapată proprietăţile şi reîncepe un nou ciclu menstrual, care debutează cu secreţia firească, pulsatorie a hormonului eliberator de gonadotropine.
Controlul Gn-RH este realizat de: opioide endogene (β-endorfine, enkefaline, dinorfine), catecolamine (adrenalină, noradrenalină), dopamină şi hormonul eliberator de corticotropine (CRH). Opioidele endogene, catecolaminele şi CRH-ul inhibă secreţia de Gn-RH, iar dopamina o stimulează. S-a descoperit o legătură de inhibiţie între complexul amigdalian cerebral (implicat în dozarea stresului), stres şi nivelurile CRH. Astfel, în situaţii de stres, amigdala cerebrală, prin intermediul neuronilor, va transmite impulsuri hipotalamusului care va secreta CRH. CRH-ul va determina eliberarea de hormon adrenocorticotrop (ACTH) din adenohipofiză care, la rândul său, va induce sinteza şi secreţia de cortizol la nivelul corticosuprarenalei. Cortizolul va determina inhibiţia Gn-RH şi, în felul acesta, scăderea ovulaţiei.
Două aspecte merită a fi aduse în discuţie.
- Primul: ciclul menstrual poate varia în cadrul populaţiei (există cazuri în care aceasta are o durată de 21 de zile sau de 40 de zile), iar, în mod fiziologic, rămâne constant la aceeaşi femeie.
- Al doilea: s-a constatat experimental că dacă secreţia de hormon eliberator de gonadotropine (Gn-RH) este continuă şi nu pulsatorie, se produce anovulaţia. [6], [10], [11]
Diagnostic şi diagnostic diferenţial
Diagnostic
În general, diagnosticul se realizează prin examenul clinic şi testele de laborator, iar acestea pot fi completate cu teste imagistice.
1. Teste de laborator
Dacă testul de sarcină este negativ, dar amenoreea şi absenţa ovulaţiei persistă, se recurge la dozarea hormonilor din sângele pacientei. Se va evalua, în primă instanţă, nivelul FSH-ului pentru a se decela eventualele disfuncţii ovariene. Nivelul normal al FSH-ului este de: 4. 17-21. 5 mUI/ml (mili-unităţi internaţionale pe mililitru). Dacă acesta depăşeşte valoarea de 25. 8 mUI/ml, specifică perioadei de postmenopauză, atunci se poate pune problema unei disfuncţii ovarine, cel mai adesea sindromul ovarelor polichistice. [12]
Se va măsura şi nivelul hormonului luteinizant (LH). Valoarea normală a acestuia este de 5-25 UI/l. O valoare mai mare decât intervalul indicat poate denota o perturbare hormonală, întâlnită în sindromul ovarelor polichistice sau în sindromul Turner. Totuşi, trebuie precizat faptul că în perioada preovulatorie (în jurul zilei a 14-a a ciclului menstrual), nivelul LH-ului poate atinge valori normale mai înalte (vârful LH), astfel momentul efectuării analizelor are o foarte mare importanţă pentru rezultatul acesteia. Mai mult, în cazul în care raportul între LH şi FSH este de 2/1 (concentraţia LH-ului este de două ori mai crescută decât cea a FSH-ului) se poate suspecta sindromul ovarelor polichistice. [13]
Se vor avea în vedere şi testele care să evalueze nivelurile estradiolului (estrogenului) şi ale progestinelor (progesteron) pentru a verifica integritatea funcţională a ovarelor.
Astfel, nivelurile normale de estrogen la femeia în perioada fertilă, sunt cuprinse în intervalul: 30-400 pg/ml. Atunci când nivelul de estrogen scade, ca, de exemplu, în cazul prezenţei unei tumori ovariene, a insuficienţei ovariene sau a sindromului Turner, atingând valori spefice perioadei de menopauză: 0-30 pg/ml, se poate pune în discuţie şi anovulaţia cronică. [14]
În privinţa progesteronului, nivelurile normale ale acestuia se încadrează în intervalul: înainte de ovulaţie, mai puţin de 1 ng/ml; la mijlocul ciclului ovarian, 5-20 ng/ml; la menopauză, mai puţin de 1 ng/ml. Dacă la femeile cu vârsta până în 40 de ani, se înregistrează la mijlocul ciclului ovarian, niveluri caracteristice perioadei preovulatorii, atunci se poate suspecta fie amenoreea, fie anovulaţia cronică. Dacă nivelurile sunt mai mari decât în mod normal, se ia de cele mai multe ori în calcul existenţa unei sarcini. Din punct de vedere patologic, cantităţi crescute de progesteron mai apar şi în: cancerele ovariene sau suprarenaliene. [15]
Pe lângă evaluarea hormonilor sexuali, pentru a evidenţia dacă anovulaţia este o consecinţă a altei maladii, se mai pot efectua teste pentru a verifica parametri în care se găsesc anumite substanţe, precum:
- TSH (hormon tireotrop): în cazul în care se suspectează că anovulaţia este consecutivă hipotirodismului sau hipertiroidismului;
- testosteron total/ testosteron liber: în cazul în care apare virilizare (caractere sexuale secundare specific masculine) şi hirsutism (pilozitate excesivă);
- prolactina: anovulaţie secundară hipeprolactinemiei (determinată de prolactinoame);
- glucoza: test de tolerenţă la glucoză (diabet zaharat, ce poate determina anovulaţie);
- cortizol cu sau fără test de stimulare la ACTH: insuficienţa suprarenaliană poate determina anovulaţie. [16]
2. Teste imagistice
Concomitent cu testele de laborator, prezentate anterior, diagnosticul poate fi pus şi pe baza testelor imagistice. În felul acesta se pot utiliza pentru diferenţierea diferitelor patologii care să conducă la anovulaţia cronică:
ultrasonografia (ecografia): transvaginală (pentru evaluarea ovarelor, cu potenţial diagnostic de sindrom al ovarelor polichistice, şi a endometrului uterin, cu evidenţierea hiperplazei endometriale) şi abdominală (glandele suprarenale);
tomografia computerizată: evaluarea integrităţii glandelor suprarenale;
rezonanţa magnetică nucleară (RMN): pentru a depista eventuale tumori hipofizare şi suprarenaliene;
densitometrie osoasă: în suspiciunea de osteoporoză (ca urmare a hipoestrogenismului). [16]
Diagnostic diferenţial
Se efectuează pentru a pune în evidenţă diferenţele între tipurile de anovulaţia cronică şi între alte patologii şi anovulaţia cronică. Astfel, anovulaţia hiperprolactinemică se va caracteriza printr-un nivel sangvin crescut de prolactină (mai mult de 20-25 ng/ml); anovulaţia hipogonadotropă va fi definită printr-o secreţie defectuoasă de gonadotropine, asociată, eventual, cu diminuarea simţului olfactiv (sindrom Kallmann); anovulaţia normogonadotropă se diferenţiază de celelalte printr-un nivel normal de estrogen, dar o secreţie deficitară de hormon stimulator de gonadotropine (Gn-RH); anovulaţia hipergonadotropă, după cum îi spune şi numele, se caracterizează printr-un nivel ridicat de gonadotropine. [2]
Din cadrul patologiilor care pot afecta funcţia ovarienă, determinând anovulaţie cronică, se pot aminti:
- boala Addison (insuficienţa suprarenaliană primară);
- tumori ale organelor sexuale interne sau externe (cu precădere cancerul endometrial);
- tumori ale glandelor suprarenale;
- hiperandrogenismul (creşterea nivelului sangvin de testosteron);
- tulburări psihiatrice: anorexia nervoasă, tulburări de anxietate, depresie;
- sindromul Cushing;
- diabetul zaharat;
- hipotiroidism;
- sarcini ectopice;
- insuficienţa ovariană. [6], [17]
Tratament
Terapia diferă de la o categorie de anovulaţie cronică la alta, astfel că metodele de tratament vor fi prezentate separat.
În anovulaţia hiperprolactinemică, întrucât hipersecreţia de prolactină este cauzată de tumori hipofizare (adenoame producătoare de prolactină/prolactinoame) se recomandă extirparea acestora, operaţia numindu-se adenomectomie hipofizară transfenoidală, cu o rată de îmbunătăţire a funcţiilor de producere şi secreţie hormonală de 50%. Alături de intervenţia chirurgicală, se poate administra un tratament medicamentos care constă în agonişti dopaminergici: bromocriptină şi cabergolină. [2], [18], [19]
Tratamentul anovulaţiei cronice hipogonadotropice presupune administrarea pulsatilă, intravenoasă, de hormon eliberator de gonadotropine (Gn-RH): o doză de 5 μg la interval de 60-90 minute în decurs de câteva zile, inducând astfel creşterea fertilităţii. În plus, pacientelor li se mai poate oferi: gonadotropină umană de menopauză (hMG) şi gonadotropina corionică umană (hCG) în cantitate de 70-150 UI/zi. De asemenea, pentru tratarea tumorilor sistemului nervos central, se recomandă intervenţiile chirurgicale. [2], [20]
În privinţa anovulaţiei normogonadotropice, variantele de tratament sunt mult mai diversificate. Se prescrie tratament antiestrogen: clomifen şi tamoxifen asociat cu medicamente pe bază de FSH recombinat, iar dacă nivelul de hormoni androgeni (testosteron) este crescut, se recomandă începerea tratamentului cu dexamethazonă. Stimularea ovariană se va realiza prin administrare de preparate gonadotropice umane. [2], [21]
Până la ora actuală, nu s-a reuşit dezvoltarea unei terapii eficiente pentru a trata anovulaţia hipergonadotropă. Dacă femeia care suferă de anovulație cronică doreşte să rămână însărcinată, singura posibilitate rămâne fertilizarea in vitro. [2], [6]
- Teste de ovulatie si trompe infundate
- Vreau un bebe
- Nu reusesc sa raman insarcinata.. infertilitate primara?
- Am facut neprotejat in a 29-a zii de menstruatie...e a 31 si inca nu i-a venit.De ce?
- Folicul dominant
- Mi-e teama k nu pot avea copii :((
- Am trompele uterine legate de 11 ani = infertilitate?
- Temperatura corpului la ovulatie.
- Cum imi pot calcula perioada fertila?
- Probleme infertilitate lipsa ovulatie